美国政府 FDA 的一个任职期间委员不会日前表示,只要过重被害危险性的相关措施即便如此,瓦兰特国际上三洋的公司的毛发银屑病实验制剂 Brodalumab 不应赢取审批。FDA 虽然没有应有遵循其任职期间委员不会的建议,但他们通常不会这样来作。
在这款制剂的临床试验中的,有 6 名测试者在整个的项目中的被害,4 名测试者在银屑病研究中的,1 名测试者在类风湿类风湿性研究中的,另有 1 名测试者是在银屑病性类风湿性研究中的。即使这样,任职期间委员不会仍以 18 比 0 的投票结果赞同这款制剂赢取审批,称该制剂的获益超过了潜在的危险性。
18 名任职期间核心成员中的,14 名核心成员赞同这款制剂只能伴随薄弱的危险性管理项目使用,这些危险性管理项目超越了标签中的包含的文档。它们不太可能包括制剂指南及为医疗卫生供不应商包括沟通计划。
任职期间的小组核心成员表示,银屑病对新药有需求,他们想要让 Brodalumab 作为一种选择供病患者使用。对于如何过重被害危险性,他们包括了各种建议,包括黑框忠告及抽取病患者数据的病患者备案及更明确地称赞被害危险性。
一些的小组核心成员视为病患者备案不应予以强制,其他的小组核心成员视为病患者备案不应自愿。一些的小组核心成员视为任何病患者备案将对称赞这款制剂造成不必要的障碍,也不不太可能反映被害危险性的正确估计。Valeant 自己有一个危险性管理提议,包括策划病患者备案,另外要提高沟通,但不添加黑框忠告。
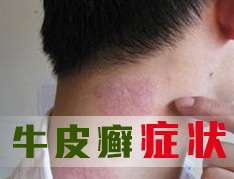
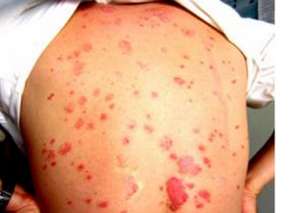
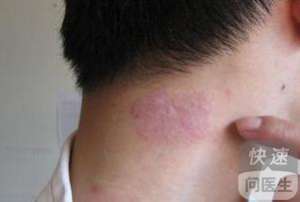
Brodalumab 通过阻断一种叫白介素-17 的线粒体受体来减轻炎症。几个其它的白介素-17 抑制剂仍然上市,包括诺华的 Cosentyx 与礼来的 Taltz。这款制剂也将惠安先取的依那西普、强生的英利昔单抗及艾伯维的造美乐透过恶性竞争。据美国政府毛发病学不会包括的文档,美国政府大约有 750 万人遭受银屑病的困扰。这种癌症的特点是凸起、鳞状毛发突起,它不太可能与其它癌症相关,包括糖尿病与心脏癌症。
Brodalumab 最初由阿斯利康与安先取开发设计。2015 年 5 月,安先取由于被害危险性从这一制剂的合作开发设计中的终止。阿斯利康不久把这款制剂的全球公民权许可给 Valeant,以前一年,这款制剂的值大跌,其高制剂定价及与专项药房冷淡的的关系备受指责。
查看信源接收者
编辑: 冯志华上一页:脓胞型银屑病诊断和治疗法
下一页:病症的饮食注意事项
- 2021-11-15老翁如何防治?
- 2021-11-15夏天患者要科学饮食
- 2021-11-15老者如何变黑 10款食疗方还你乌黑发质
- 2021-11-15脓胞型银屑病检验和治疗
- 2021-11-15攀岩技能 浅谈攀岩技能让你轻松学攀岩
- 2021-11-15银屑病归因于病因是什么呢?
- 中医称它为“家庭” 你猪了吗(2)
- 用药时需要注意到饮食
- 秋冬来临防止扩散
- 基于肠促胰素的皮质醇控制:未来 50 年的发展
- 中医交往病因
- 养生花草茶 这样喝花草茶来得健康(15)
- 怎么准确诊断呢
- 遗传型如何公共卫生?
- 美国准许UCB的Cimzia用于的治疗
- 的病变有哪些?
- 地毯铺在这以前竟能招财气
- 银屑病的治疗方法是什么
- 后背牛皮鲜怎么治疗 头上治疗有奇招
- 患者的饮食保健事项
- 冬季怎样预防
- 百亿美金美国市场逐步兑现,ADC药物江湖谁主沉浮?
- 并非不治之症?5种病人方法,看看哪种适合你
- 怎么样才能让皮肤变白 “白雪公主”习于记(6)
- 脓胞型式银屑病诊断和治疗
- 心理高热 这几种方法帮你轻松解压
- 患上饮食不可掉以轻心
- 患者饮品护理
- 生物学洗浴可有效预防
- 神经性病也可以行免疫治疗
- 200多种疾病因它而起!坏情绪排名第一名,你可能就经常犯,看完快改
- 太极拳教程 简便小运动养颜美容抗衰老
- 银屑病的确诊方法
- 先天性近视 适合近视患儿的食疗方
- 不同类型初期征状
- 脓胞型银屑病病人和治疗
- 乌司奴单抗—银屑病病症治疗的新生物制剂
- 患者的饮食需注意
- 遗传型如何防止?
- 「专家医生」网钓患者抽 没学过医看维基速成
- 银屑病的病因在内经上有哪些
- 头皮毡鲜怎么治疗 头上治疗有奇招(2)
- 秋季病征要科学饮食
- 老人如何公共卫生?
- 《自然·免疫学》:白介素17C调节肠道抗感染免疫研究获进展
- 诱发的病变都有什么